Chapter 4: Kp, Kc & Le-Chatelier's Principle
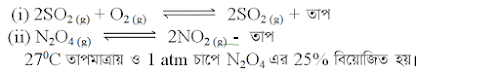 [ঢাকা, দিনাজপুর, সিলেট, যশোর বোর্ড-২০১৮]
[ঢাকা, দিনাজপুর, সিলেট, যশোর বোর্ড-২০১৮](ক) ভনেগার কী?
(খ) মাখনকে পানিমুক্ত করা প্রয়োজন কেন?
(গ) (ii) নং বিক্রিয়াটির Kp এর মান নির্ণয় করো।
(ঘ) তাপমাত্রা বাড়ালে উদ্দীপকের কোন বিক্রিয়ায় সর্বাধিক উৎপাদ পাওয়া যাবে? বিশ্লেষণ করো।
১নং প্রশ্নের উত্তর
(ক) ইথানয়িক এসিডের 6-10% জলীয় দ্রবণকে ভিনেগার বলে।
(খ) বাণিজ্যিক বাটার বা মাখনে প্রধানত 80-82% চর্বি, 16-17% পানি ও 0.8% দুগ্ধ প্রোটিনসহ 1-2% খাদ্য লবণ (NaCl) প্রিজারভেটিভসরূপে মিশ্রিত থাকে। মাখনের স্বাদের জন্য এ পরিমাণ পানি থাকা প্রয়োজন। কিন্তু এর চেয়ে বেশি পানি থাকলে ঐ অধিক পানিতে দুগ্ধ প্রোটিন ও ল্যাকটোজ মাখনকে সহজেই অণুজীবের আক্রমনের উপযোগী করে পচনশীল করে। ফলে মাখনের স্থায়িত্ব কমে যায় ও নষ্ট হয়। তাই মাখন থেকে পানি অপসারণ করা অপরিহার্য ।


(i) নং বিক্রিয়াটির বৈশিষ্ট্যঃ (i) উভমুখী বিক্রিয়া ।
(ii) তাপোৎপাদী বিক্রিয়া ।
(iii) আয়তন সংকোচন বা মোল সংখ্যার হ্রাস ঘটে।
(iv) গ্যাসীয় বিক্রিয়া ।
লা- শাতেলিয়ার নীতিঃ কোন বিক্রিয়ার সাম্যাবস্থায় যদি কোন নিয়ামক ( তাপ, চাপ, ঘনমাত্রা ইত্যাদি) পরিবর্তন করা হয়, তবে সাম্যের অবস্থান এমনভাবে পরিবর্তিত হয় যেন নিয়ামক পরিবর্তনের ফলাফল প্রশমিত হয়।
তাপমাত্রার প্রভাবঃ
উদ্দীপকের (i) নং বিক্রিয়াটি উভমুখী ও তাপোৎপাদী বিক্রিয়া। এ বিক্রিয়া যখন সামনের দিকে ঘটে তখন তাপ উৎপন্ন হয়। আর যখন পেছনের দিকে ঘটে তখন তাপ শোষিত হয়। এ বিক্রিয়ায় যদি তাপ প্রয়োগ করা হয় তাহলে লা- শাতেলিয়ার নীতি অনুসারে তাপ বৃদ্ধিজনিত ফলাফল প্রশমিত করার জন্য বিক্রিয়াটির সাম্যাবস্থা বাম দিকে সরে যাবে। অর্থাৎ কিছু SO3 বিয়োজিত হয়ে SO2 এ পরিণত হবে।
অতএব, তাপমাত্রা বাড়ালে উদ্দীপকের (i) নং বিক্রিয়ায় উৎপাদ হ্রাস পাবে।
(ii) নং বিক্রিয়ার বৈশিষ্ট্যঃ (i) উভমুখী বিক্রিয়া ।
(ii) তাপহারী বিক্রিয়া ।
(iii) আয়তনের প্রসারণ বা মোল সংখ্যার বৃদ্ধি ঘটে।
(iv) গ্যাসীয় বিক্রিয়া ।
তাপমাত্রার প্রভাবঃ
উদ্দীপকের (ii) নং বিক্রিয়াটি তাপহারী বলে যখন বিক্রিয়াটি সামনের দিকে ঘটে তখন তাপ শোষিত হয়। আর যখন পেছনের দিকে ঘটে তখন তাপ উৎপন্ন হয়। এ বিক্রিয়ায় যদি তাপ বৃদ্ধি করা হয় তাহলে লা- শাতেলিয়ার নীতি অনুসারে তাপ বৃদ্ধিজনিত ফলাফল প্রশমিত করার জন্য বিক্রিয়াটির সাম্যাবস্থা ডান দিকে স্থানান্তরিত হবে। অর্থাৎ N2O4 বিয়োজিত হয়ে NO2 এর উৎপাদন বৃদ্ধি পাবে।
অতএব, উদ্দীপকের ((ii) নং বিক্রিয়ায় তাপমাত্রা বাড়ালে উৎপাদ সর্বাধিক হবে।
২।
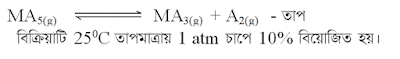
[ঢাকা, দিনাজপুর, সিলেট, যশোর বোর্ড-২০১৮]
(খ) CaCl2 এবং MgCl2 এর মধ্যে কোনটির গলনাংক বেশি এবং কেন?
(গ) উদ্দীপকের বিক্রিয়াটির Kp এর মান নির্ণয় করো।
(ঘ) বিক্রিয়াটির সাম্যাবস্থায় তাপমাত্রা ও চাপের পরিবর্তন ঘটলে উৎপাদের উপর কীরূপ প্রভাব ফেলে?
২নং প্রশ্নের উত্তর
(ক) পরমাণুর ইলেকট্রন শক্তি শোষণ করে নিম্ন শক্তিস্তর থেকে উচ্চ শক্তিস্তরে গমন করে। আবার শক্তি বিকিরণ করে উচ্চ শক্তিস্তর থেকে নিম্ন শক্তিস্তরে ফিরে আসে। এ বিকীর্ণ শক্তিকে বিশ্লেষণ করলে এর মধ্যে বিভিন্ন বর্ণের সমাহার পাওয়া যায় । বিভিন্ন বর্ণের এ সমাহারকে বর্ণালী বলে।
(খ) CaCl2 এবং MgCl2 এর মধ্যে CaCl2 এর গলনাংক বেশি।
এটি ফাযানের নীতির আলোকে ব্যাখ্যা করা যায়। ফাযানের নীতি হলো-
(i) ক্যাটায়নের আকার যত ক্ষুদ্র হয়
(ii) অ্যানায়নের আকার যত বড় হয়
(ii) ক্যাটায়ন ও অ্যা নায়নের চার্জ যত বেশি হয়
এবং (iv) যদি আনায়নের ও আরবিটালে ইলেকট্রন থাকে,
তবে পোলারায়ণের মাত্রা অধিক হয় এবং আয়নিক যৌগের সমযোজী বৈশিষ্ট বৃদ্ধি পায়।
CaCl2 এবং MgCl2 উভয় যৌগই আয়নিক প্রকৃতির। এদের মধ্যে
একই অ্যানায়ন (Cl-) রয়েছে এবং
এদের ক্যাটায়নের চার্জও (Ca2+ ও Mg2+) সমান।
কিন্তু Mg2+ এর আকার Ca2+ এর তুলনায় ছোট। ফলে ফাযানে নীতি
অনুসারে MgCl2 যৌগে পোলারায়ণ বেশি ঘটে এবং সমযোজী প্রকৃতি বৃদ্ধি পায়।
অপরপক্ষে, Ca2+ এর আকার Mg2+ এর আকারের তুলনায় বড় বলে CaCl2 এ পোলারায়ণ কম ঘটে এবং এটি অধিক মাত্রায়
আয়নিক বা তড়িৎযোজী । সেই কারণে CaCl2 এর তুলনায় MgCl2 এর গলনাংক
কম। অর্থাৎ CaCl2 এর গলনাংক MgCl2 এর গলনাংক বেশি।
বিক্রিয়াটির বৈশিষ্ট্যঃ (i) উভমুখী বিক্রিয়া ।
(ii) তাপহারী বিক্রিয়া ।(iii) আয়তনের প্রসারণ বা বৃদ্ধি ঘটে।
(iv) গ্যাসীয় বিক্রিয়া ।
লা- শাতেলিয়ার নীতিঃ কোন বিক্রিয়ার সাম্যাবস্থায় যদি কোন নিয়ামক ( তাপ, চাপ, ঘনমাত্রা ইত্যাদি) পরিবর্তন করা হয়, তবে সাম্যের অবস্থান এমনভাবে পরিবর্তিত হয় যেন নিয়ামক পরিবর্তনের ফলাফল প্রশমিত হয়।
তাপমাত্রার প্রভাবঃ
উদ্দীপকের প্রদত্ত বিক্রিয়াটি উভমুখী ও তাপহারী বিক্রিয়া। এ বিক্রিয়া যখন সামনের দিকে ঘটে তখন তাপ শোষিত হয়। আর যখন পেছনের দিকে ঘটে তখন তাপ উৎপন্ন হয়। এ বিক্রিয়ায় যদি তাপ প্রয়োগ করা হয় তাহলে লা- শাতেলিয়ার নীতি অনুসারে তাপ বৃদ্ধিজনিত ফলাফল প্রশমিত করার জন্য বিক্রিয়াটি সামনের দিকে ঘটবে। অর্থাৎ MA5 বিয়োজিত হয়ে MA3 ও A2 উৎপন্ন হবে। আবার তাপ হ্রাস করা হলে তাপ হ্রাসজনিত ফলাফল প্রশমিত করার জন্য বিক্রিয়াটি পেছনের দিকে ঘটবে। অর্থাৎ MA3 ও A2 বিক্রিয়া করে MA5 উৎপন্ন করে। সুতরাং উদ্দীপকের বিক্রিয়ায় তাপমাত্রা বৃদ্ধি করলে সাম্য বাম থেকে ডানে সরে যাবে অর্থাৎ উৎপাদ বৃদ্ধি পাবে এবং তাপমাত্রা হ্রাস করলে সাম্যআবস্থা ডান থেকে বামে সরে যাবে অর্থাৎ উৎপাদ হ্রাস পাবে।
চাপের প্রভাবঃ রাসায়নিক বিক্রিয়ার সাম্যাবস্থায় বিক্রিয়কের মোট মোল সংখ্যা এবং উৎপাদের মোট মোল সংখ্যার পরিবর্তন হলে সাম্যাবস্থার উপর চাপের প্রভাব পরিলক্ষিত কয়।
উপরের উভমুখী বিক্রিয়ায় ডান দিকে উৎপাদের মোল সংখ্যা বেশি (1+1=2 মোল) এবং বাম দিকে বিক্রিয়কের মোল
সংখ্যা কম (1 মোল)। এ
বিক্রিয়ায় যদি চাপ প্রয়োগ করা হয় তাহলে লা- শাতেলিয়ার নীতি অনুসারে চাপ বৃদ্ধিজনিত
ফলাফল প্রশমিত করার জন্য বিক্রিয়াটি পেছনের দিকে ঘটবে। অর্থাৎ MA3 ও
A2 বিক্রিয়া করে MA5 উৎপন্ন করবে। আবার চাপ হ্রাস করা
হলে চাপ হ্রাসজনিত ফলাফল প্রশমিত করার জন্য বিক্রিয়াটি সামনের দিকে ঘটবে। অর্থাৎ MA5 ভেঙ্গে MA3 ও
A2 উৎপন্ন হবে। সুতরাং এই বিক্রিয়ার
সাম্যাবস্থায় চাপ বৃদ্ধি করলে সাম্য ডান দিক থেকে বাম দিকে সরে যাবে অর্থাৎ উৎপাদ
হ্রাস পাবে এবং চাপ হ্রাস করলে সাম্য বাম থেকে ডানে সরে যাবে অর্থাৎ উৎপাদ বৃদ্ধি
পাবে।
৩। অ্যামোনিয়ার শিল্পোৎপাদন বিক্রিয়াটি নিম্নরূপঃ
ঢাকা বোর্ডঃ ২০১৭
(ক)
(খ) ‘সকল অবস্থান্তর মৌল d- ব্লক মৌল, কিন্তু
সকল d-ব্লক মৌল অবস্থান্তর মৌল নয়’- কেন?
(গ)
উদ্দীপকের বিক্রিয়ার Kp নির্ণয় কর।
(ঘ) উদ্দীপকের বিক্রিয়া হতে সর্বোচ্চ
উৎপাদ পাওয়ার শর্তসমূহ বিশ্লেষণ কর।
৩ নং প্রশ্নের উত্তর
(ক) কোন দ্রবণে হাইড্রোজেন আয়নের (H+) মোলার
ঘনমাত্রার ঋণাত্মক লগারিদলকে ঐ দ্রবণের pH
(খ) আমরা জানি, যে সকল মৌলের ইলেকট্রন বিন্যাসে সর্বশেষ ইলেকট্রনগুলো সর্ববহিঃস্থ শক্তিস্তরের পূর্ববর্তী স্তরের d-অরবিটালে প্রবেশ করে তাদেরকে ব্লক মৌল বলে। পক্ষারন্তরে, যে সকল d-ব্লক মৌলের স্থিতিশীল আয়নের d-অরবিটাল আংশিকভাবে (d1-9) পূর্ণ থাকে তাদেরকে অবস্থান্তর মৌল বলে। যেমন, নিচের ইলেকট্রন বিন্যাসগুলো লক্ষ করি-
উপরের ইলেকট্রন বিন্যাস থেকে দেখা যায় যে, প্রত্যেকটি মৌলই d-ব্লক মৌল। কিন্তু স্ক্যান্ডিয়ামের স্থিতিশীল আয়ন Sc3+ এর ইলেকট্রন বিন্যাসে কোন d-অরবিটাল নেই। আবার জিংকের স্থিতিশীল আয়ন Zn2+ এর d-অরবিটাল সম্পূর্ণ পূর্ণ। তাই Sc ও Zn উভয়ই d-ব্লক মৌল হলেও অবস্থান্তর মৌল নয়। অপরপক্ষে, আয়রণের স্থিতিশীল আয়ন Fe3+ এর d-অরবিটালে 5টি ইলেকট্রন রয়েছে। তাই Fe একই সাথে d-ব্লক ও অবস্থান্তর মৌল।
অতএব, উল্লেখিত কারণে বলা যায় ‘সকল অবস্থান্তর মৌল d- ব্লক মৌল, কিন্তু সকল d-ব্লক মৌল অবস্থান্তর মৌল নয়’।
(ii)
তাপোৎপাদী বিক্রিয়া ।
(iii) মোল সংখ্যার সংকোচন বা হ্রাস ঘটে।
(iv)
গ্যাসীয় বিক্রিয়া ।
লা- শাতেলিয়ার নীতিঃ কোন বিক্রিয়ার সাম্যাবস্থায় যদি কোন নিয়ামক ( তাপ, চাপ,
ঘনমাত্রা ইত্যাদি) পরিবর্তন করা হয়, তবে সাম্যের অবস্থান এমনভাবে পরিবর্তিত হয় যেন
নিয়ামক পরিবর্তনের ফলাফল প্রশমিত হয়।
তাপমাত্রার প্রভাবঃ
উদ্দীপকের শিল্পোৎপাদন বিক্রিয়াটি তাপোৎপাদী বিক্রিয়া। এ বিক্রিয়া যখন সামনের
দিকে ঘটে তখন তাপ উৎপন্ন হয়। আর যখন পেছনের দিকে ঘটে তখন তাপ শোষিত হয়। এ
বিক্রিয়ায় যদি তাপ প্রয়োগ করা হয় তাহলে লা- শাতেলিয়ার নীতি অনুসারে তাপ বৃদ্ধিজনিত
ফলাফল প্রশমিত করার জন্য বিক্রিয়াটি পেছনের দিকে ঘটবে। অর্থাৎ NH3 ভেঙ্গে
N2 ও H2 উৎপন্ন করে।
আবার তাপ হ্রাস করা হলে তাপ হ্রাসজনিত ফলাফল প্রশমিত করার জন্য বিক্রিয়াটি সামনের
দিকে ঘটবে। অর্থাৎ N2 ও H2 বিক্রিয়া করে NH3 উৎপন্ন
হবে।
কিন্তু নিম্ন তাপমাত্রায় অ্যামোনিয়া উৎপাদনের হার বা গতি হ্রাস পায় । তাই
শিল্পক্ষেত্রে NH3 উৎপাদন
লাভজনক করার জন্য অত্যানুকূল তাপমাত্রা 4500-5500 C ব্যবহার করা হয়।
চাপের প্রভাবঃ রাসায়নিক বিক্রিয়ার
সাম্যাবস্থায় বিক্রিয়কের মোট মোল সংখ্যা এবং উৎপাদের মোট মোল সংখ্যার পরিবর্তন হলে
সাম্যাবস্থার উপর চাপের প্রভাব থাকবে।
উপরের উভমুখী বিক্রিয়ায় ডান দিকে মোল সংখ্যা কম (2 মোল) এবং বাম দিকে মোল সংখ্যা বেশি (1+3=4 মোল)। এ
বিক্রিয়ায় যদি চাপ প্রয়োগ করা হয় তাহলে লা- শাতেলিয়ার নীতি অনুসারে চাপ বৃদ্ধিজনিত
ফলাফল প্রশমিত করার জন্য বিক্রিয়াটি সামনের দিকে ঘটবে। অর্থাৎ N2 ও H2 বিক্রিয়া করে NH3 উৎপন্ন
করবে। সুতরাং লা- শাতেলিয়ার নীতি অনুসারে
এই বিক্রিয়ার সাম্যাবস্থায় চাপ বৃদ্ধি করলে সাম্যাবস্থা ডান দিকে সরে যাবে অর্থাৎ
উৎপাদ বৃদ্ধি পাবে। কিন্তু অত্যধিক চাপ সৃষ্টি ব্যয়বহুল বলে
এক্ষেত্রে 200- 250 atm চাপ প্রয়োগ করলে অ্যামোনিয়ার সর্বোচ্চ উৎপাদন
লাভজনক হবে।
প্রভাবকের ব্যবহারঃ বিক্রিয়ার বেগ বৃদ্ধি করার জন্য প্রভাবক হিসেবে আয়রণ চূর্ণ এবং প্রভাবক সহায়ক হিসেবে KOH ও Al2O3 এর মিশ্রণ ব্যবহার করা হয়।
অতএব উল্লেখিত পদক্ষেপ গ্রহণ করলে সর্বোচ্চ অ্যামোনিয়া পাওয়া যাবে।
৪।
কুমিল্লা বোর্ডঃ ২০১৭
(গ) উদ্দীপকের বিক্রিয়াটির Kp এর মান নির্ণয় কর
(ঘ) সাম্যাবস্থায় বিক্রিয়াটিতে তাপ ও চাপের পরিবর্তন ঘটলে উৎপাদের পরিমানের পরিবর্তন ঘটবে কিনা?
বিশ্লেষণ কর।
৪
নং প্রশ্নের উত্তর
(ক) কাছাকাছি স্ফুটনাংক বিশিষ্ট দুই বা ততোধিক তরল পদার্থের
মিশ্রণকে অংশ কলামযুক্ত একটি পাতন ফ্লাস্কে তাপ প্রয়োগ করে উপাদানগুলোকে নিজ নিজ
স্ফুটনাংকে পাতিত করে পৃথক করার পদ্ধতিকে আংশিক পাতন বলে।
(খ) না, Zn
অবস্থান্তর মৌল নয়।
আমরা জানি, যে সকল মৌলের ইলেকট্রন বিন্যাসে সর্বশেষ ইলেকট্রনগুলো সর্ববহিঃস্থ
শক্তিস্তরের পূর্ববর্তী স্তরের d-অরবিটালে প্রবেশ করে তাদেরকে ব্লক মৌল বলে।
পক্ষারন্তরে, যে সকল d-ব্লক মৌলের স্থিতিশীল আয়নের d-অরবিটাল আংশিকভাবে (d^1-9) পূর্ণ থাকে তাদেরকে অবস্থান্তর
মৌল বলে।
এখন Zn এর ইলেকট্রন
বিন্যাস লক্ষ করি -
উপরের ইলেকট্রন বিন্যাস থেকে দেখা যায় যে, Zn d-ব্লক মৌল। কিন্তু জিংকের স্থিতিশীল আয়ন Zn2+ এর d-অরবিটাল সম্পূর্ণ পূর্ণ (3d^10) । ফলে Zn d-ব্লক মৌল হলেও অবস্থান্তর মৌল নয়।
বিক্রিয়াটির
বৈশিষ্ট্যঃ (i) উভমুখী বিক্রিয়া ।
(ii) তাপহারী
বিক্রিয়া ।
(iii) আয়তনের প্রসারণ ঘটে।
(iv) গ্যাসীয় বিক্রিয়া ।
লা- শাতেলিয়ার নীতিঃ কোন বিক্রিয়ার সাম্যাবস্থায় যদি কোন
নিয়ামক ( তাপ, চাপ, ঘনমাত্রা ইত্যাদি) পরিবর্তন করা হয়, তবে সাম্যের অবস্থান
এমনভাবে পরিবর্তিত হয় যেন নিয়ামক পরিবর্তনের ফলাফল প্রশমিত হয়।
তাপমাত্রার প্রভাবঃ
উদ্দীপকের বিক্রিয়াটি উভমুখী ও তাপহারী বিক্রিয়া। এ বিক্রিয়া যখন সামনের দিকে ঘটে তখন তাপ শোষিত হয়। আর যখন পেছনের দিকে ঘটে তখন তাপ উৎপন্ন হয়। এ বিক্রিয়ায় যদি তাপ প্রয়োগ করা হয় তাহলে লা- শাতেলিয়ার নীতি অনুসারে তাপ বৃদ্ধিজনিত ফলাফল প্রশমিত করার জন্য বিক্রিয়াটি সামনের দিকে ঘটবে। অর্থাৎ PCl5 বিয়োজিত হয়ে PCl3 ও Cl2 উৎপন্ন হবে। আবার তাপ হ্রাস করা হলে তাপ হ্রাসজনিত ফলাফল প্রশমিত করার জন্য বিক্রিয়াটি পেছনের দিকে ঘটবে। অর্থাৎ PCl3 ও Cl2 পরষ্পর বিক্রিয়া করে PCl5 উৎপন্ন করে। সুতরাং উদ্দীপকের বিক্রিয়ায় তাপ প্রয়োগ করলে সাম্যের অবস্থান বাম দিকে থেক ডান দিক সরে যায় অর্থাৎ উৎপাদ বৃদ্ধি পায় এবং তাপ হ্রাস করলে সাম্যের অবস্থান ডান থেকে বামে সরে যায় অর্থাৎ উৎপাদ হ্রাস পায়।
চাপের প্রভাবঃ রাসায়নিক বিক্রিয়ার সাম্যাবস্থায় বিক্রিয়কের মোট মোল সংখ্যা এবং উৎপাদের মোট মোল সংখ্যার পরিবর্তন হলে সাম্যাবস্থার উপর চাপের প্রভাব থাকবে।
উপরের উভমুখী বিক্রিয়ায় ডান দিকে মোল সংখ্যা বেশি (1+1=2 মোল) এবং বাম দিকে মোল সংখ্যা কম (1 মোল)। এ
বিক্রিয়ায় যদি চাপ প্রয়োগ করা হয় তাহলে লা- শাতেলিয়ার নীতি অনুসারে চাপ বৃদ্ধিজনিত
ফলাফল প্রশমিত করার জন্য বিক্রিয়াটি পেছনের দিকে ঘটবে। অর্থাৎ PCl3 ও
Cl2
বিক্রিয়া করে PCl5 উৎপন্ন হবে। আবার চাপ হ্রাস করা
হলে চাপ হ্রাসজনিত ফলাফল প্রশমিত করার জন্য বিক্রিয়াটি সামনের দিকে ঘটবে। অর্থাৎ PCl5
ভেঙ্গে PCl3 ও
Cl2
উৎপন্ন হবে। সুতরাং লা- শাতেলিয়ার নীতি অনুসারে এই
বিক্রিয়ার সাম্যাবস্থায় চাপ বৃদ্ধি করলে সাম্যের অবস্থান ডান দিক থেকে বাম দিকে
সরে যাবে অর্থাৎ উৎপাদ হ্রাস পাবে এবং চাপ হ্রাস করলে সাম্যের অবস্থান বাম থেকে
ডানে সরে যাবে অর্থাৎ উৎপাদ বৃদ্ধি পাবে।










কোন মন্তব্য নেই